Репродуктивная функция пары оценивается не только по состоянию здоровья женщины. Ровно в половине случаев причиной незачатия является недостаточное качество спермы. Репродуктолог назначит обоим партнерам обследование, на основании которого даст рекомендации по улучшению биоматериалов.
Содержание
Обследование в репродуктологии
Мужчинам, имеющим проблемы с зачатием, врач назначает тщательное исследование. Исключаются патологии, влияющие на качество и количество спермы в эякуляте:
- гормональная дисфункция;
- преждевременное семяизвержение;
- варикозное расширение вен;
- врожденные аномалии репродуктивных органов;
- воспаление мочевыводящей системы, простатит;
- новообразования;
- острые воспалительные состояния.
Заболевания, передающиеся половым путем, могут повлиять на качество спермы и привести к мужскому бесплодию: гарднерелла, трихомониаз, хламидиоз, уреаплазмоз, вирусные инфекции.
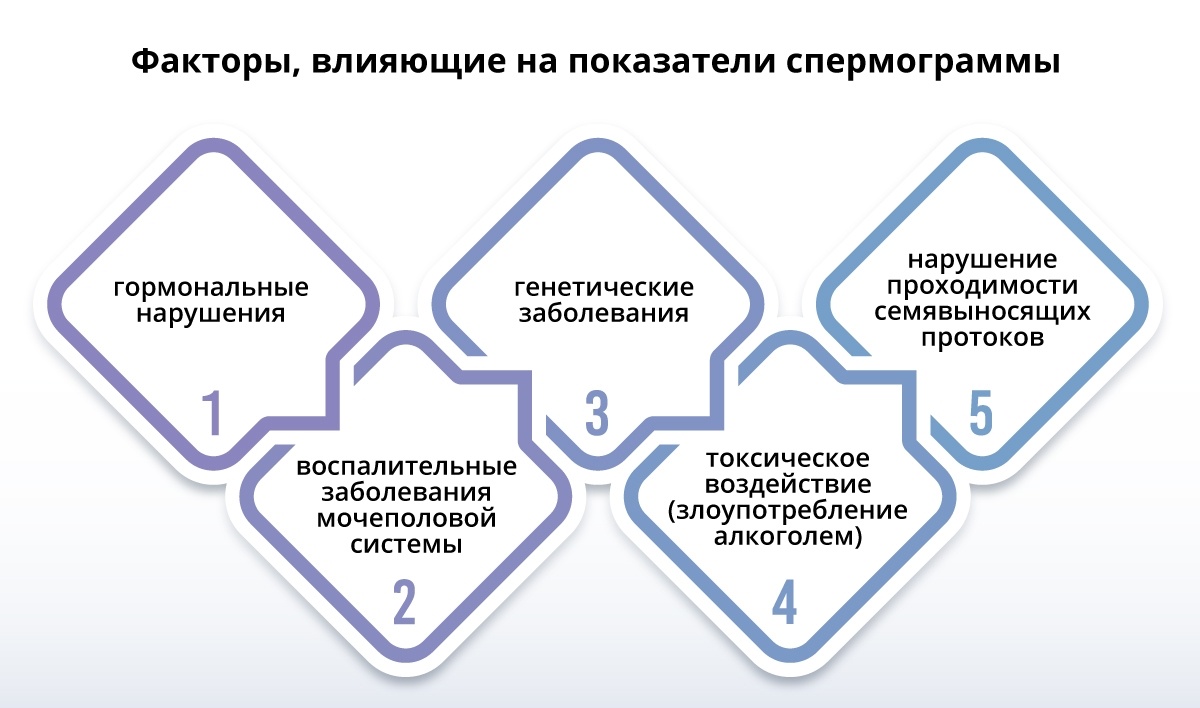
Как определить качество спермы с помощью методов лабораторной диагностики:
- Тест MAR является основным методом определения иммунного бесплодия;
- фрагментация ДНК — оценка цепей ДНК;
- биохимия сперматозоидов — дает общую клиническую картину состояния сперматозоидов;
- EMIS — для оценки функциональных патологий.
На начальных этапах обследования врач может назначить общую спермограмму для оценки количества, подвижности сперматозоидов, соотношения в составе эякулята. Дополнительным диагностическим инструментом станет УЗИ мошонки, предстательной железы и мочевыводящей системы.
Как улучшить качество спермы: лучшие методы
Чтобы повлиять на мужскую фертильность, важно незамедлительно воздействовать на все факторы, влияющие на качество и количество сперматозоидов:
- Качество спермы снижается из-за стресса, поэтому следует избегать тяжелых стрессовых состояний.
- Ухудшение качества спермы приводит к хроническому недосыпанию, низкой физической активности, нарушению сна и бодрствованию.
- Рацион необходимо скорректировать, чтобы максимально использовать полезные компоненты.
- Откажитесь от алкоголя, курения, наркотиков, фастфуда и чрезмерно жирной жареной пищи.
По решению врача будут назначены препараты и витамины для улучшения качества спермы, дополнительные процедуры.
Продукты для повышения качества спермы
На качественные показатели положительно влияют такие вещества в рационе будущего отца:
- омега-3 жирные кислоты;
- футбол;
- цинк;
- бета-каротин;
- витамины D, C, E.
Самостоятельно назначать БАД и препараты не стоит — их избыток приводит к нарушению половой функции.

В пище содержится большое количество этих веществ:
- бобовые;
- жирная морская рыба;
- морковь;
- тыква;
- персики;
- абрикосы;
- свежая зелень;
- овсянка;
- гречиха;
- курица, индейка.
В случае проблем с весом рекомендуется снизить массу тела до нормальных значений. Красное мясо негативно влияет на подвижность сперматозоидов, поэтому в период планирования малыша стоит дополнить рацион птицей и рыбой.
Воздержание и качество спермы
Согласно рекомендации ВОЗ, продолжительность воздержания не должна превышать 4 дней. Качество спермы ухудшается с 5-го дня, ее будет недостаточно для зачатия здорового ребенка. Воздержание менее 2 дней не рекомендуется: объема эякулята может быть недостаточно для зачатия за пределами окна фертильности женщины.
Комплексные рекомендации
Вот несколько советов, которые помогут вам улучшить качество спермы для зачатия:
- предотвращать и предотвращать заболевания: качество спермы после коронавируса, вирусных и острых респираторных заболеваний намного хуже;
- избегайте синтетического и ломкого белья, не пропускающего влагу — белье изготавливается только из натуральных материалов, бесплатно;
- не злоупотребляйте длительными горячими ваннами, сауной, парной;
- откажитесь от интенсивных физических нагрузок в пользу нормальной повседневной активности: плавания, ходьбы.
В клинике доктора АкНера он выполняет полное обследование мужской репродуктивной системы, анализ спермы и успешно лечит любые обнаруженные отклонения. Обращайтесь к квалифицированным врачам с многолетним опытом лечения урологических заболеваний — мы вносим свой вклад в счастливое отцовство!














































Главное меню
Главное меню
Эндокринологические аспекты хронического цистита у женщин Часть 1. Общие эндокринологические аспекты
Инфекции нижних мочевых путей у женщин — актуальная медико-социальная проблема современной амбулаторной урологии, в основном из-за высокой частоты их распространения среди женского населения . По статистике, ежегодно около 15% сексуально активных женщин страдают хотя бы одним эпизодом острого бактериального цистита и в целом не менее 60% женщин страдали этим заболеванием хотя бы раз в жизни [1]. После острого бактериального цистита примерно у 50% женщин в течение года развиваются рецидивы заболевания, которые в 15-25% случаев переходят в хронический рецидивирующий бактериальный цистит (CRBC), который часто приобретает очень стойкое клиническое течение и характеризуется недостаточной эффективностью фармакотерапевтических мероприятий, что часто сопровождается тяжелой медицинской, социальной и психологической дезадаптацией и резким снижением качества жизни женщин 2.
HRBC: СОВРЕМЕННЫЕ ПРОБЛЕМЫ АНТИМИКРОБНОЙ ХИМИОТЕРАПИИ И ПУТИ ИХ РЕШЕНИЯ
В настоящее время практически все исследователи и клиницисты отмечают многофакторность явления снижения эффективности антибактериальной терапии при CRBC:
- Факторы, вызываемые микроорганизмами (способность бактерий образовывать биопленки (биопленки) в слизистой оболочке мочевого пузыря; мутации, приводящие к увеличению экспрессии ключевых ферментов, разлагающих антибиотики, которые бактерии могут передавать последующим поколениям штаммов; модификация структуры эндо и экзотоксины, синтезируемые бактериями и т д.) [5, 6].
- Факторы со стороны макроорганизма (снижение механизмов естественной и приобретенной иммунологической реактивности, как врожденной, так и приобретенной в течение жизни в связи с различными заболеваниями (например, снижение уротелиального синтеза секреторных иммуноглобулинов IgA и защитных гликозаминогликанов слизистых оболочек) ; повышенный уровень аллергической активации населения, что делает практически невозможным назначение антибиотиков в ряде случаев при хронических заболеваниях, сопровождающихся потенциальной способностью изменять метаболизм антибиотика в организме (заболевания печени и желудочно-кишечного тракта); желудочно-кишечный тракт) и т д через) [7,8].
- Фармакологические факторы (практически полное отсутствие синтеза новых эффективных классов антибиотиков в последние десятилетия, ограниченный механизм действия некоторых противомикробных химиопрепаратов, бесконтрольное и нерациональное назначение антибиотиков в клинической практике, использование некачественных дженериков, повсеместное назначение антибиотиков ветеринарами животных, что приводит к последующей сенсибилизации иммунной системы человека при употреблении мяса таких животных и т д.) 11.
Глобальная волна устойчивости к антибиотикам в различных ее проявлениях, захлестнувшая подавляющее большинство стран мира, в том числе и Россию, вынуждает сегодня активно искать пути решения проблемы фармакотерапии инфекционных заболеваний, в том числе CRBC у женщин. И если в настоящее время возможности синтеза новых антибиотиков, эффективных для борьбы с микроорганизмами, остаются ограниченными, то, конечно, следует обратить внимание на состояние второго участника инфекционно-воспалительного процесса — макроорганизма, противостоящего любому возбудителю и результату заражения инфекционное воспаление не зависит от каждого из них в отдельности, а является результатом их противостояния и взаимодействия, опосредованного огромным количеством механизмов с обеих сторон. Эта позиция, на наш взгляд, особенно применима к мочевому пузырю, который с физиологической точки зрения не является простым «пассивным» резервуаром для удержания и эвакуации мочи, а является гормонозависимым органом, все структуры которого являются под мощным нейрогормональным контролем [12]. Опосредованное, в основном, половыми стероидными гормонами влияние на анатомо-функциональное состояние структурных элементов мочевого пузыря выполняет практически все его физиологические функции: от резервуара-резервуара и эвакуации до уротелиозащитного, нейроэндотелиального (иннервация и кровоснабжение) и выше вся бактерицидная функция, которая в сообществе обеспечивает уротелий мочевого пузыря известный и достаточно высокий уровень естественной антибактериальной устойчивости [13, 14].
Зависимость анатомо-функционального состояния уротелия мочевого пузыря у женщин от уровня половых гормонов была установлена еще в 1947 г. [15]. В дальнейших исследованиях показана ключевая роль половых гормонов (эстрогена и прогестерона) в обеспечении синтеза уротелием защитных мукополисахаридов-гликозаминогликанов (гиалуроновой кислоты и ее солей натрия и цинка, хондроитинсульфата, гликопротеинов, муцина), которые вызывают антибактериальная защита слизистой оболочки мочевого пузыря (антиадгезивный фактор), потеря которого естественным образом увеличивает восприимчивость уротелия к различным неблагоприятным воздействиям, в том числе инфекционным агентам. Сегодня это считается одним из ключевых проявлений уротелиальной дисфункции, лежащей в основе современного патогенеза CRBC и его рецидивов 19.
Работы последних десятилетий свидетельствуют о том, что CRBC — это не столько самостоятельный локальный инфекционно-воспалительный процесс в мочевом пузыре, сколько инфекционная «верхушка айсберга» системных метаболических и гормональных механизмов (хроническое системное цитокиновое воспаление, вегетативная симпатическая гиперактивность, оксидативный стресс, снижение антиоксидантной и иммунологической реактивности организма, нейроэндотелиальная дисфункция, системная гипоксия и др.), что неизбежно влияет на ключевые функции мочевого пузыря, в том числе бактерицидные 22.
С точки зрения системного подхода к проблеме CRBC также очевидно, что при общем плохом самочувствии женщины частота ее рецидивов имеет тенденцию к увеличению, что может быть связано с высокой частотой гормональных системных нарушений обмена веществ у женщин население современных женщин (ожирение, инсулинорезистентность, дислипидемия, артериальная гипертензия (эндотелиальная дисфункция), сахарный диабет 2 типа, саркопения (дефицит количества и качества мышечной массы), дефицит витамина D и т д.). Эти изменения имеют тенденцию к омоложению и, учитывая увеличение средней продолжительности жизни женщин на Земле, будут сопровождать ее почти всю вторую половину ее жизни после наступления менопаузы, постоянно прогрессируя одновременно с ухудшением состояния анатомического состояния и функции мочевого пузыря с возрастом («старение мочевого пузыря», или «сенильный пузырь») [23, 24].
ЭНДОКРИН-АВТОКРИН-ПАРАКРИННАЯ МОДЕЛЬ РЕГУЛЯЦИИ МОЧЕВОГО ПУЗЫРЯ КАК ПАТОГЕНЕТИЧЕСКАЯ ОСНОВА КОНТРОЛЯ CRHC У ЖЕНЩИН
На сегодняшний день накоплено огромное количество клинических и экспериментальных научных публикаций, позволяющих утверждать, что мочевой пузырь представляет собой единую функциональную систему, элементы которой (уротелиальные клетки, нервные окончания, сосуды, миоциты и миофибробласты) находятся в постоянной взаимодействующей активности направлен на поддержание физиологической податливости органа, чтобы гарантировать его максимально оптимальные функции в постоянно меняющихся условиях внешней и внутренней среды. Уротелиальные и другие клетки мочевого пузыря могут активироваться или блокироваться различными механизмами, как системными (эндокринными), так и местными (аутокринными или паракринными) [20].
Эндокринная регуляция мочевого пузыря, как и всех других органов, осуществляется специализированными веществами разной природы — гормонами, синтезируемыми в специализированных эндокринных железах и поступающими через системный кровоток в клетки органов и тканей, в которых выражены соответствующие рецепторы (регуляция к расстояние). Ключевая роль половых гормонов (эстроген, прогестерон, андрогены), витамина D и инсулина в обеспечении метаболизма и энергетического обмена во всех клетках мочевого пузыря теперь продемонстрирована (экспрессия в мочевом пузыре соответствующих рецепторов гормонов), и важная роль в этом также была сыграна показаны: процесс гормона сна (мелатонин), гормон роста (соматотропин), который проявляет свои физиологические эффекты через аналогичный фактор роста инсулин-1 (IGF-1), а также гормоны жировой ткани (лептин, адипонектин, адипсин, резистин, десмин и др.), который сегодня считается одним из наиболее активных эндокринных органов [25–33].
Эндокринная регуляция мочевого пузыря выполняет почти все свои функции, создавая «гормональный» плацдарм для реализации механизмов аутокринной и паракринной регуляции, присущих клеткам, которые также происходят в тканях мочевого пузыря. При аутокринной регуляции клетка способна к самостоятельному синтезу местного гормона (гормоноподобного вещества) и в то же время имеет для него соответствующие рецепторы. Другими словами, клетка одновременно является продуцентом гормона и клеткой-мишенью. Примером может служить эндотелин, продуцируемый эндотелиальными клетками, также в сосудах мочевого пузыря, который непосредственно влияет на функцию самих эндотелиальных клеток [34]. Паракринная регуляция означает, что биологически активные вещества (местные гормоны), выделяемые продуцирующими клетками, диффундируют в ткани и действуют на близлежащие клетки-мишени. Так, например, работают многие митогенные стимуляторы (факторы роста полипептидов) — эпидермальный фактор роста (EGF), фактор роста тромбоцитов (PRT), интерлейкин-2 (фактор роста Т-клеток), фактор роста нервов (NGF) и т.д. [34].
известно, что стимуляция рецепторов и мембранных каналов на уротелиальных клетках может привести к высвобождению многих медиаторов, регулирующих функции нервных окончаний и других типов клеток мочевого пузыря. С другой стороны, клетки уротелия сами по себе могут быть мишенями для медиаторов, высвобождаемых клетками нейротелия, эндотелия или других типов клеток. Высвобождение местных медиаторов в тканях мочевого пузыря осуществляется за счет адаптивного взаимодействия симпатической и парасимпатической частей вегетативной нервной системы с участием системных и местных гормональных механизмов (нейроэндокринная регуляция), что позволяет мочевому пузырю , морфологически состоящие из различных типов клеток, чтобы функционировать как единая функциональная клетка синцития [20] (Рис. 1).
В этой слаженной функциональной системе важная роль отводится эндокринному компоненту вегетативной регуляции функций мочевого пузыря, поскольку гормоны оказывают как прямое влияние на анатомо-функциональное состояние всех структурных элементов мочевого пузыря, так и опосредованно, посредством регулирует функциональную активность и экспрессию различных рецепторов в уротелии и нервно-мышечных элементах детрузора. Результаты исследований показывают, что половые гормоны способны модулировать функции местного нейрорецепторного аппарата мочевого пузыря как у мужчин, так и у женщин. Таким образом, известно, что у женщин эффекты эстрогена проявляются через модуляцию активности и экспрессии преимущественно α-адренорецепторов сосудов мочевого пузыря и воздействия прогестерона через β-адренорецепторы детрузора [35].
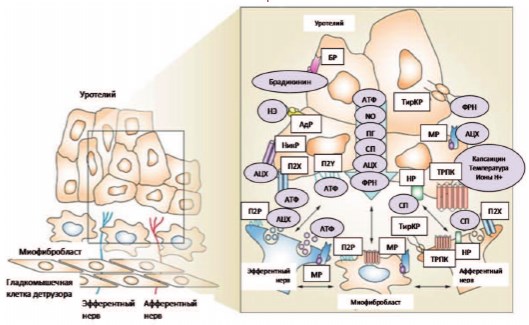
Рис. 1. Гипотетическая модель взаимодействия уротелиальных клеток (уротелия), афферентных и эфферентных нервных окончаний (нейротелий), сосудов (эндотелий), гладкомышечных клеток и миофибробластов мочевого пузыря [20].
Сокращения: АТФаденозинтрифосфат NRнейрокининовый рецептор PG — простагландины ACh — ацетилхолиновый NikRникотиновый рецептор JV — субстанция P ADR — адренергический рецептор NO — оксид азота TirKRтирозинкиназный рецептор BRбрадикининовый рецептор Аффинный рецептор MRR пурпиновый рецепторный рецептор BRбрадикиновый рецептор MRR аффинный рецептор NE P2X и P2Y — потенциальные пуринергические каналы NGF — подтипы X и Y рецепторов фактора роста нервов
Следовательно, половые стероидные гормоны играют одну из важнейших ролей в метаболизме мочевого пузыря, регулируя почти все его функции; поэтому рассматривать различные клинические варианты заболеваний мочевого пузыря, в том числе инфекционные и воспалительные, в отрыве от его гормональной регуляции, кажется нелогичным и некорректным.
Стероидные половые гормоны у женщин: синтез и характеристика динамики возраста. В настоящее время медицина разработала традиционную неправильную концепцию половых гормонов, согласно которой предполагается, что существуют только «мужские» (андрогены) или только «женские» (эстроген, прогестерон) половые гормоны, использование которых нецелесообразно, недопустимо и даже опасно для противоположного пола. Однако с биохимической точки зрения это неверно, так как все половые гормоны являются представителями одного семейства гормонов — стероидных гормонов (которые также включают глюкокортикоиды, минералокортикоиды и витамин D) и имеют уникальный биохимический предшественник (7-дигидрохолестерин) [35,36] (рис. 2).
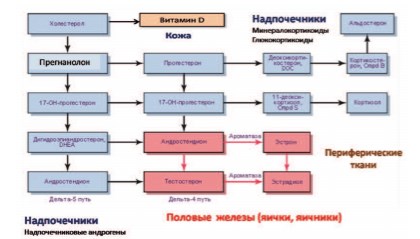
Рис. 2. Схема синтеза и биотрансформации половых стероидных гормонов у мужчин и женщин [35, 36]
В связи с этим традиционное разделение половых гормонов на «женские» и «мужские» следует считать неправильным и неправильным, поскольку для обеспечения всех физиологических процессов и мужчинам, и женщинам необходимо наличие в организме всех трех половых гормонов а также витамин D в соответствующих физиологических концентрациях, необходимых организму [36,37].
Результаты современных исследований демонстрируют важную роль всех трех половых гормонов в регуляции различных физиологических процессов у женщин (транскрипция, связывание металлов и ДНК, внутриклеточная передача сигналов, активация генов синтеза белков, метаболизм углеводов и жиров, функционирование клеточного митохондрии и т д.). В этих процессах участвуют как эстроген (активация рецепторов эстрогена приводит к модуляции экспрессии примерно 600 генов), так и прогестерон (активация рецепторов прогестерона вызывает модуляцию примерно 1800 генов), и андрогены (активация рецепторов андрогенов приводит к изменения экспрессии около 250 генов) [37] (рис. 3).
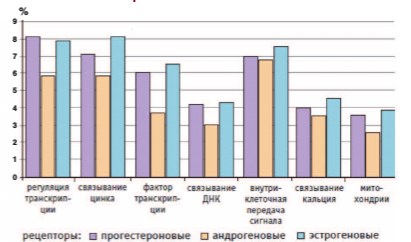
Рис. 3. Процент генов основных категорий, функциональных по отношению к активации различных стероидных рецепторов у женщин [37]
Активация рецепторов витамина D приводит к модуляции экспрессии не менее 300 генов (по другим данным до 2000 генов), что является отражением крайней физиологической важности постоянства баланса витамина D в организме, поскольку этот витамин, являясь фактически активным стероидным гормоном, регулирует по крайней мере 3% генома человека, включая гены рецептора инсулина, метаболизм глюкозы и стероидогенез 38. С возрастом уровень всех трех половых гормонов и витамина D снижается у обоих полов, что совпадает с началом формирования и прогрессирования большинства возрастных заболеваний, в том числе мочеполовых путей [41]. Следовательно, с возрастом у ранее здоровых урологически женщин могут возникать различные симптомы нарушений мочеполовой системы, которых не было в более молодом возрасте (стрессовое недержание мочи, гиперактивный мочевой пузырь, никтурия, рецидивирующие воспалительные заболевания мочевого пузыря и т.д.). 43.
Ранее традиционно считалось, что различные мочеполовые расстройства у женщин связаны только с дефицитом эстрогена и в связи с этим относят к среднесрочным проявлениям климактерического синдрома, которые развиваются вскоре после его первых проявлений (приливы и вазомоторные расстройства). [45]. Однако сейчас эта точка зрения была радикально пересмотрена, и современная концепция эндокринологии у женщин заключается в том, что им (как и мужчинам) необходимо воздействие всех трех половых гормонов, уровни которых постепенно снижаются с возрастом [41]. При этом первым гормональным дефицитом у женщин сегодня считается дефицит прогестерона, который можно наблюдать уже в 35 лет, и поэтому уровень андрогенов у женщин начинает снижаться, что приводит к снижению почти вдвое возраст 40 лет по сравнению с возрастом 20 [41, 46]. С 40-45 лет, когда большинство женщин вступает в менопаузальный переход, и вплоть до менопаузы в среднем в 51 год у женщин начинается снижение синтеза эстрогенов, что проявляется различными проявлениями дефицита эстрогенов (климактерический синдром) [47, 48].
Кроме того, в каждом временном интервале по мере уменьшения синтеза и эффектов соответствующего полового гормона могут наблюдаться различные клинические проявления нижних мочевыводящих путей, анатомия которых у женщин отличается от мужской анатомии (короткая и широкая уретра, близость влагалища и уретры к потенциальному источнику инфекции — анальному отверстию и т синтез различных биологических секретов из слизистых оболочек половых органов и нижних мочевых путей с помощью местных защитных факторов (муцин, лизоцим, IgA, IgS, мукополисахариды, гликозаминогликаны и др.), которые обычно считаются гормонозависимыми процессами [49–51] . Это положение подтверждается широко известным в классической урогинекологии фактом, согласно которому существует надежная взаимосвязь между частотой и выраженностью нарушений гормонально-синтетической функции яичников, с одной стороны, и дисфункциями мочевого пузыря у женщин, с другой стороны [52, 53].
ЗАКЛЮЧЕНИЕ
В современных условиях возрастающей антибиотикорезистентности большинства уропатогенов, вызывающих хронические рецидивирующие инфекции нижних мочевых путей у женщин, остается очень ограниченное количество противомикробных химиотерапевтических препаратов для эффективного решения проблемы CRBC. Однако клиническая практика показывает, что даже их рациональное использование по показаниям не позволяет многим пациентам проводить эффективную санацию мочевого пузыря и успешно снижать частоту рецидивов CRBC. Роль микроорганизма в патогенезе любого инфекционно-воспалительного процесса неоспорима, но сегодня следует уделять больше внимания второй стороне взаимодействия в рамках хронического рецидивирующего инфекционного воспаления, а именно состоянию макроорганизма. Мочевой пузырь у женщин является гормонозависимым органом, и нормальный клеточный уровень гормонов, по-видимому, является одним из ключевых условий, необходимых для поддержания всех физиологических функций мочевого пузыря, включая его естественную антибактериальную функцию. Современная эндокринно-аутокринно-паракринная теория регуляции функции мочевого пузыря позволяет рассматривать CRBC как своего рода инфекционно-бактериальную «верхушку айсберга» гормонального нарушения здоровья мочевого пузыря у женщин. Быстрое и эффективное управление эндокринологическими механизмами регуляции функций мочевого пузыря у женщин может стать одним из наиболее эффективных фармакотерапевтических вариантов лечения и профилактики любых инфекций нижних мочевых путей у женщин, включая CRBC.
ЛИТЕРАТУРА
1. Набер К.Г., Чо Й.Х., Мацумото Т., Шефер А.С. Иммуноактивная профилактика рецидивирующих инфекций мочевыводящих путей: метаанализ. Int J Antimicrob 2009; 2: 111-119.
2. Лоран О.Б., Зайцев А.Б., Годунов Б.Н. Особенности диагностики и лечения хронического цистита у женщин. Акушерство и гинекология 2000; (3): 40-43.
3. Франк В. Антибактериальная терапия в амбулаторной практике. М .: ГЭОТАР-Медиа, 2010. 256 с.
4. Перепанова Т.С. Инфекции почек и мочевыводящих путей: современные подходы к терапии. Аптека. 2004; 82 (3-4): 16-21.
5. Палагин И.С., Сухорукова М.В., Дехнич А.В., Эйдельштейн М.В., Шевелев А.Н., Гринев А.В и др. исследовательская группа «ДАРМИС». Современное состояние антибиотикорезистентности возбудителей внебольничных инфекций мочевыводящих путей в России: результаты исследования DARMIS (2010-2011). Клиническая микробиология. Антимикробная химиотерапия 2012; 14 (4): 280-302.
6. Minardi D, d’Anzeo G, Cantoro D. Инфекции мочевыводящих путей у женщин: этиология и варианты лечения. Стажер J General Med 2011; 4: 333-334.
7. Аписарнтанарак А., Буппунхарун В., Тиенгрим С., Саванпаньялерт П., Ашвапоки Н. Обзор моделей чувствительности к антимикробным препаратам для грамотрицательных бактерий из программы Национального надзора за устойчивостью к противомикробным препаратам Таиланда (NARST) с 2000 по 2005 годы. J Med Assoc Thai 2009; 92 (Приложение 4): 91-94.
8. Стрельцова О.С., Крупин В.Н. Хронический цистит: новизна в диагностике и лечении. Лечащий врач 2008 г .; (7): 18-24.
9. Сидоренко С.В., Тишков В.И. Молекулярные основы устойчивости к антибиотикам. Успехи в биологической химии 2004 г .; 44 (3): 263-306.
10. Gissen IC. Европейский Союз уделяет особое внимание насосам: Европейские академии наук (EASAC) рекомендуют сильную исследовательскую поддержку для борьбы с устойчивостью к антибактериальным препаратам. Clin Microbiol Infect 2008; 14 (10): 889-891.
11. Аллокати Н., Масулли М., Алексеев М.Ф., Ди Илио К. Escherichia coli в Европе: обзор. Int J Environ Res Public Health 2013; 10 (12): 6235-6254.
12. Андерссон К.Е., Арнер А. Сокращение и расслабление мочевого пузыря: физиология и патофизиология. Physiological Reviews 2004; 84 (3): 935-986.
13. Робинсон Д., Туз-Хобсон П., Кардозо Л. Влияние гормонов на нижние мочевыводящие пути. Menopause Int 2013; 19 (4): 155-162.
14. Аподака Г. Уроэпителий: не просто пассивный барьер. Трафик 2004; 5 (3): 117-128.
15. Cifuentes L. Эпителий вагинального типа в женском трине; клиническая проблема тригонита. J Urol 1947; 57 (6): 1028-1037.
16. Парсонс CL. Роль мочевого эпителия в патогенезе цистита / простатита / интерстициального уретрита. Уроло 2007; 69 (доп. 4): 9-16.
17. Lilly JD, Parsons CL. Гликозаминогликаны на поверхности мочевого пузыря являются барьером проницаемости эпителия человека. Хирургия, гинекология и акушерство 1990; 171 (6): 2543-2551.
18. Грэм Э., Чай Т.С. Уротелий мочевого пузыря и дисфункция уротелиальных клеток мочевого пузыря при инрестициальном цистите. Curr urol rep 2006; 7 (6): 440-446.
19. Сивик К.Е., Мобли Х.Л. Война с уропатогенной кишечной палочкой: возвращение в мочевыводящие пути [мини-обзор]. Infect Immun 2010; 78 (2) 2: 568-585.
20. Бирдер Л.А., де Гроат WC. Механизмы заболевания: участие уротелия в дисфункции мочевого пузыря. Нат Клин Практ Урол 2007; 4 (1): 46-54.
21. Гровер С., Шривастава А., Ли Р., Тевари А.К., Те А.Е. Роль воспаления в функции мочевого пузыря и интерстициальный цистит. Ther Adv Urol 2011; 3 (1): 19-33.
22. Ханг Л., Вулт Б., Шен З. Репертуар цитокинов эпителиальных клеток, выстилающих мочевыводящие пути человека. J Urol 1998; 159 (6): 2185-2192.
23. Банн Ф., Кирби М., Пинкни Э., Кардозо Л., Чаппл С., Честер К и др. исть ли связь между гиперактивным мочевым пузырем и метаболическим синдромом у женщин? Систематический обзор наблюдательных исследований. Int J Clin Pract. 2015; 69 (2): 199-217.
24. Singh S, van Herwijnen I., Phillips C. Управление низкими урогенитальными изменениями в менопаузе. Menopause Int 2013; 19 (2): 77-81.
25. Тюзиков И.А., Калинченко С.Ю., Апетов С.С. Андрогенная недостаточность у женщин в урогинекологической практике: патофизиологические механизмы, клинические «маски» и фармакотерапия трансдермальными формами тестостерона. Вестник акушера-гинеколога России. 2014; (1): 33-43.
26. Ханна-Митчелл А.Т., Робинсон Д., Кардозо Л., Эвераерт К., Петков Г.В. Нужно ли нам больше знать о влиянии гормонов на дисфункцию нижних мочевыводящих путей? ICI-RS 2014. Neurourol Urodyn 2016; 35 (2): 299-303.
27. Чен Дж., Чжоу Ю. X., Ю Ю. Л., Шен З. Дж. Влияние половых гормонов на функцию и структуру мочевого пузыря: эксперимент с овариэктомированными самками крыс. Чжунхуа И Сюэ За Чжи 2008; 88 (26): 1851-1854.
28. Шапиро Б., Редман Т.Л., Звара П. Влияние аналога витамина D на функцию мочевого пузыря и сенсорную передачу сигналов в моделях цистита на животных. Уроло 2013; 81 (2): 466-470.
29. Фатхоллахи А., Данешгари Ф., Ханна-Митчелл А. Т.. Мелатонин и его роль в функции нижних мочевыводящих путей: обзор статьи. Curr Urol 2015; 8 (3): 113-118.
30. Мессинг Э.М., Бубберс Дж. Э., Декернион Дж. Б., Фэхи Дж. Л.. Рост-стимулирующая активность, производимая клетками рака мочевого пузыря человека. J Urol 1984; 132 (6): 1230-1234.
31. Руссо Г.И., Кастелли Т., Урзи Д., Привитера С., Ла Виньера С., Кондорелли Р.А и др. иовые связи между ненейрогенными симптомами нижних мочевыводящих путей, вторичными по отношению к доброкачественной обструкции простаты, метаболическому синдрому и его компонентам: систематический обзор. Int J Urol 2015; 22 (11): 982-990.
32. Мэтьюз CA. Факторы риска недержания мочи, кала или двойного недержания мочи у женщин. Curr Opin Obstet Gynecol 2014; 26 (5): 393-397.
33. Грир WJ, Richter HE, Bartolucci AA, Burgio KL. Ожирение и расстройства тазового дна: систематический обзор. Obstet Gynecol 2008; 112 (2, Pt 1): 341-349.
34. Солодков А.С., Сологуб Е.Б. Физиология человека. 2-е изд., Перераб. И доп. М .: Олимпия Пресс, 2005. 528 с.
35. Хакер Н., Мур Дж. Г., Гамбон Дж. [Ред.]. Основы акушерства и гинекологии. Saunders, 2004. 544 с.
36. Ворслов Л.О., Тюзиков И.А., Тишова Ю.А., Калинченко С.Ю., Гусакова Д.А. Квартет здоровья — это новая концепция современной профилактической и эстетической медицины: половые гормоны у женщин, возможности внутреннего и наружного применения. Косметика и медицина. 2016; (2): 26-34.
37. Торшин И. Ю., Громова О. А., Сухих Г. Т., Галицкая С. А., Юргеев И. С. Молекулярные механизмы дидрогестерона (Дюфастон®). Полногеномное исследование транскрипционных эффектов рецепторов прогестерона, андрогенов и эстрогенов. Consilium Medicum. Гинекология 2009; 11 (5): 9-16.
38. Castro LC. Эндокринная система витамина D. Arq Bras Endocrinol Metabol. 2011; 55 (8): 566-575.
39. Шварц Г.Я. Витамин D и D-гормон. М .: Анахарсис, 2005. 152 с.
40. Холик MF, Бинкли NC, Бишофф-Феррари HA. Оценка, лечение и профилактика дефицита витамина D: Руководство по клинической практике эндокринного общества. JClin Endocrinol. Metab 2011; 96 (7): 1911-1930.
41. Бабер Р.Дж., Панай Н., Фентон А. Авторская группа IMS. Рекомендации IMS по здоровью женщин среднего возраста и гормональной терапии в период менопаузы. Климатический 2016; 19 (2): 109-150.
42. Тюзиков А.А., Греков А.А., Апетов С.С., Ворслов, Л.О. Калинченко С.Ю. Ноктурия: современные гендерные аспекты эпидемиологии, патогенеза и диагностики. Экспериментальная и клиническая урология. 2013; (3): 113-122.
43. Тюзиков И.А., Калинченко С.Ю., Тишова Ю.А., Ворслов Л.О., Греков Е.А. Ноктурия как актуальная междисциплинарная проблема интегративной медицины XXI века: эпидемиология и взаимосвязь с возрастными сопутствующими заболеваниями. Клиническая нефрология. 2014; (5): 48-55.
44. Тюзиков И.А. Эндокринологические аспекты патогенеза и фармакотерапии хронического неинфекционного урогенитального болевого синдрома у женщин. Эффективная фармакотерапия. Эндокринология. 2014; (9): 44-56.
45. Стурди Д. В., Пайнс А., Арчер Д. Ф., Бабер Р. Дж., Барлоу Д., Биркхойзер М. Х и др. ибновленные рекомендации IMS по гормональной терапии в постменопаузе и стратегиям профилактики для здоровья людей среднего возраста. Климатический 2011; 14 (3): 302-320.
46. Шифрен Дж. Л., Ханфлинг С. Сексуальность в среднем возрасте и за его пределами: Специальный отчет о состоянии здоровья. Гарвардский университет: Harvard Health Publications, Бостон, Массачусетс. 2010 г.
47. Лян С.К., Ли Т.Х., Чанг С.Д. Влияние половых гормонов на пролиферацию клеток и апоптоз в мышцах мочевого пузыря крыс, подвергшихся овариэктомии. Тайвань J Obstet Gynecol 2013, 52 (3): 335-340.
48. Серов В.Н., Прилепская В.Н., Овсянникова Т.В. (Ред.). Гинекологическая эндокринология. М .: МЕДпресс-информ, 2015. 512 с.
49. Mirmonsef P, Hotton AL, Gilbert D, Gioia CJ, Maric D, Hope TJ и др. ировни гликогена в неразбавленной половой жидкости и их взаимосвязь с pH влагалища, эстрогеном и прогестероном. PLoS One 2016; 11 (4): e0153553.
50. Mirmonsef P, Modur S, Burgad D, Gilbert D, Golub ET, French AL, et al. Исследовательское сравнение уровней гликогена влагалища и Lactobacillus у женщин в пременопаузе и постменопаузе. Менопауза 2015; 22 (7): 702-709.
51. Деннерштейн Г.Дж., Эллис Д.Х. Эстроген, гликоген и вагинальный кандидоз. Aust NZJ Obstet Gynaecol 2001; 41 (3): 326-328.
52. Монтесума Т., Антониу Ф.И., Роса де Силва А.С., Са М.Ф., Ферриани Р.А., Феррейра С.Х. Оценка симптомов недержания мочи у женщин с синдромом поликистозных яичников. Клиники (Сан-Паоло) 2011; 66 (11): 1911-1915.
53. Hvidman L, Foldspang A, Mommsen S, Bugge Nielsen J. Менструальный цикл, использование женских гормонов и недержание мочи у женщин в пременопаузе. Int Urogynecol J Дисфункция тазового дна 2003; 14 (1): 56-61.
